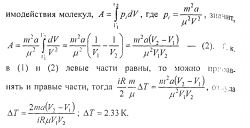6.16. Для водорода силы взаимодействия между молекулами незначительны; преимущественную роль играют собственные размеры молекул. Написать уравнение состояния такого полу-идеального газа. Какую ошибку мы допустим при нахождении количества водорода v, находящегося в некотором объеме при температуре t = 0° С и давлении р = 280 МПа, не учитывая собственного объема молекул? 6.17. В сосуде объемом V = 10 л находится масса m = 0,25 кг азота при температуре t = 27° С. Какую часть давления газа составляет давление, обусловленное силами взаимодействия молекул? Какую часть объема сосуда составляет собственный объем молекул?
6.18. Количество v = 0,5 кмоль некоторого газа занимает объем V1=1м3. При расширении газа до объема V2 = 1.2 м3 была совершена работа против сил взаимодействия молекул A = 5,684 кДж. Найти постоянную а, входящую в уравнение Ван-дер-В аальса.
6.19. Масса m = 20 кг азота адиабатически расширяется в вакуум от объема V1 = 1 м3 до объема V2 = 1 м3. Найти понижение температуры DT при этом расширении, считая известной для азота постоянную а, входящую в уравнение Ван-дер-Ваальса (смотри ответ 6.2).
6.20. Количества v = 0,5 кмоль трехатомного газа адеабатически расширяется в вакуум от объема V1 = 0,5м3 до объема V2 = 3 м3 Температура газа при этом понижается на DТ = 122 К. Найти постоянную а, входящую в уравнение Ван-дер-Ваальса.
6.18. Количество v = 0,5 кмоль некоторого газа занимает объем V1=1м3. При расширении газа до объема V2 = 1.2 м3 была совершена работа против сил взаимодействия молекул A = 5,684 кДж. Найти постоянную а, входящую в уравнение Ван-дер-В аальса.
6.19. Масса m = 20 кг азота адиабатически расширяется в вакуум от объема V1 = 1 м3 до объема V2 = 1 м3. Найти понижение температуры DT при этом расширении, считая известной для азота постоянную а, входящую в уравнение Ван-дер-Ваальса (смотри ответ 6.2).
6.20. Количества v = 0,5 кмоль трехатомного газа адеабатически расширяется в вакуум от объема V1 = 0,5м3 до объема V2 = 3 м3 Температура газа при этом понижается на DТ = 122 К. Найти постоянную а, входящую в уравнение Ван-дер-Ваальса.